Bài 6: ĐỊNH LUẬT BOYLE. ĐỊNH LUẬT CHARLES
I. TRẠNG THÁI VÀ QUÁ TRÌNH BIẾN ĐỔI TRẠNG THÁI CỦA CHẤT KHÍ
– Trạng thái của 1 khối lượng khí không đổi được xác định bằng 3 thông số (gọi là thông số trạng thái):
+ Thể tích V
+ Áp suất p
+ Nhiệt độ tuyệt đối T
– Quá trình khối khí biến đổi từ trạng thái này sang trạng thái khác gọi là quá trình biến đổi trạng thái.
– Quá trình biến đổi trạng thái của một khối lượng khí xác định mà trong đó có 1 thông số trạng thái không đổi gọi là đẳng quá trình.
+ Quá trình đẳng nhiệt: là quá trình biến đổi trạng thái mà trong đó nhiệt độ được giữ không đổi.
+ Quá trình đẳng áp: là quá trình biến đổi trạng thái mà trong đó áp suất được giữ không đổi.
+ Quá trình đẳng tích: là quá trình biến đổi trạng thái mà trong đó thể tích được giữ không đổi.
II. QUÁ TRÌNH ĐẲNG NHIỆT – ĐỊNH LUẬT BOYLE
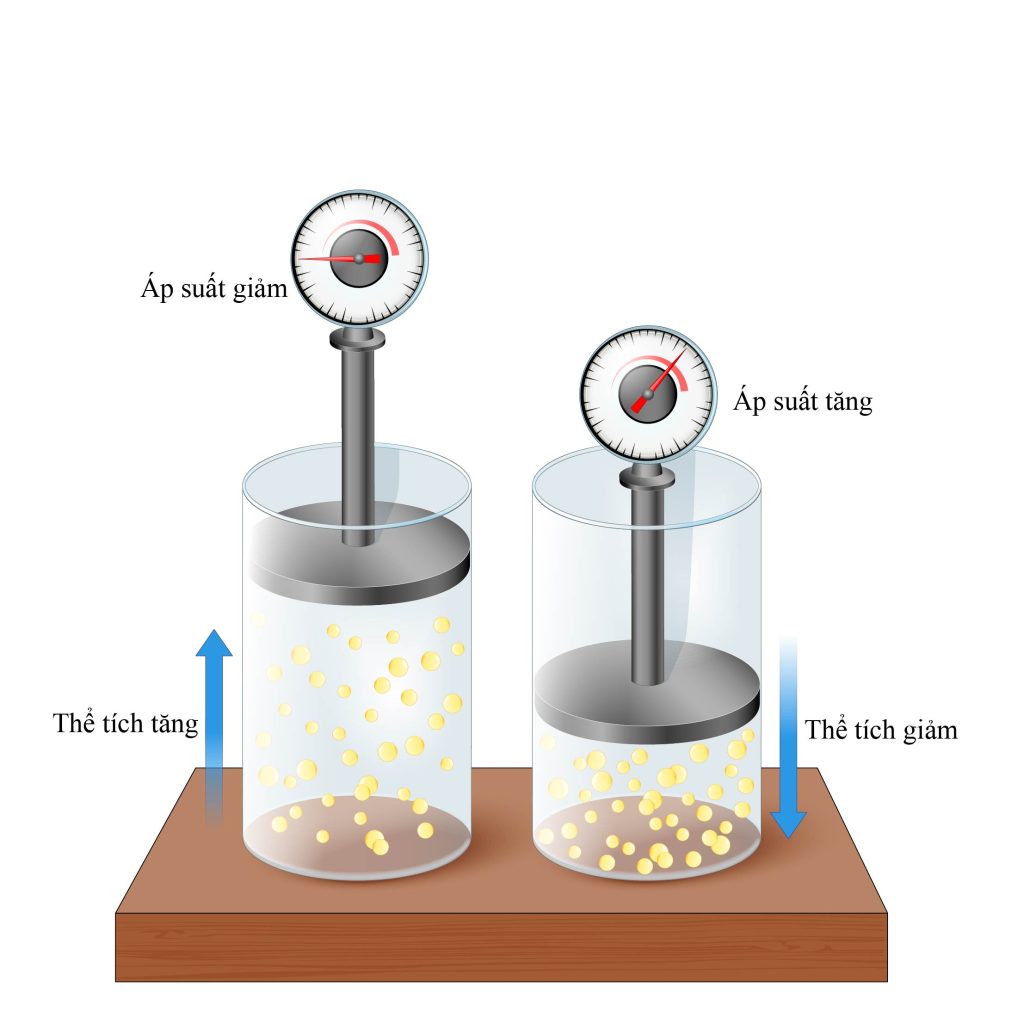
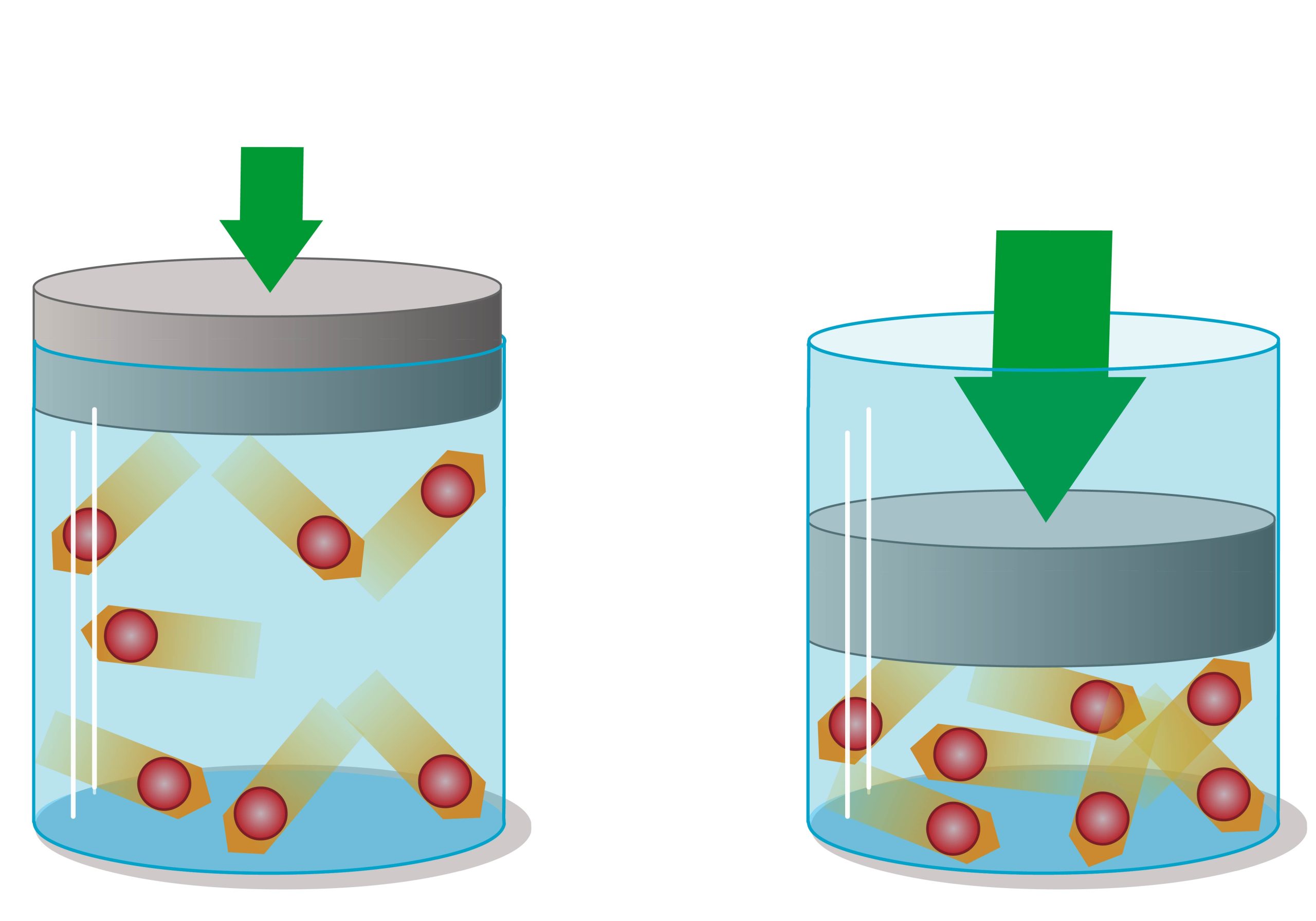
1. Định luật Boyle
Ở nhiệt độ không đổi, áp suất của một khối lượng khí xác định tỉ lệ nghịch với thể tích của nó.
\(pV = \) hằng số
hay:
\({p_1}{V_1} = {p_2}{V_2}\)
2. Đường đẳng nhiệt
– Đường đẳng nhiệt là đường biểu diễn sự biến thiên của áp suất theo thể tích khi nhiệt độ không đổi.
– Trong hệ toạ độ (Op; OV), đường đẳng nhiệt là đường hypebol.
– Ứng với các nhiệt độ khác nhau của cùng một lượng khí có các đường đẳng nhiệt khác nhau.
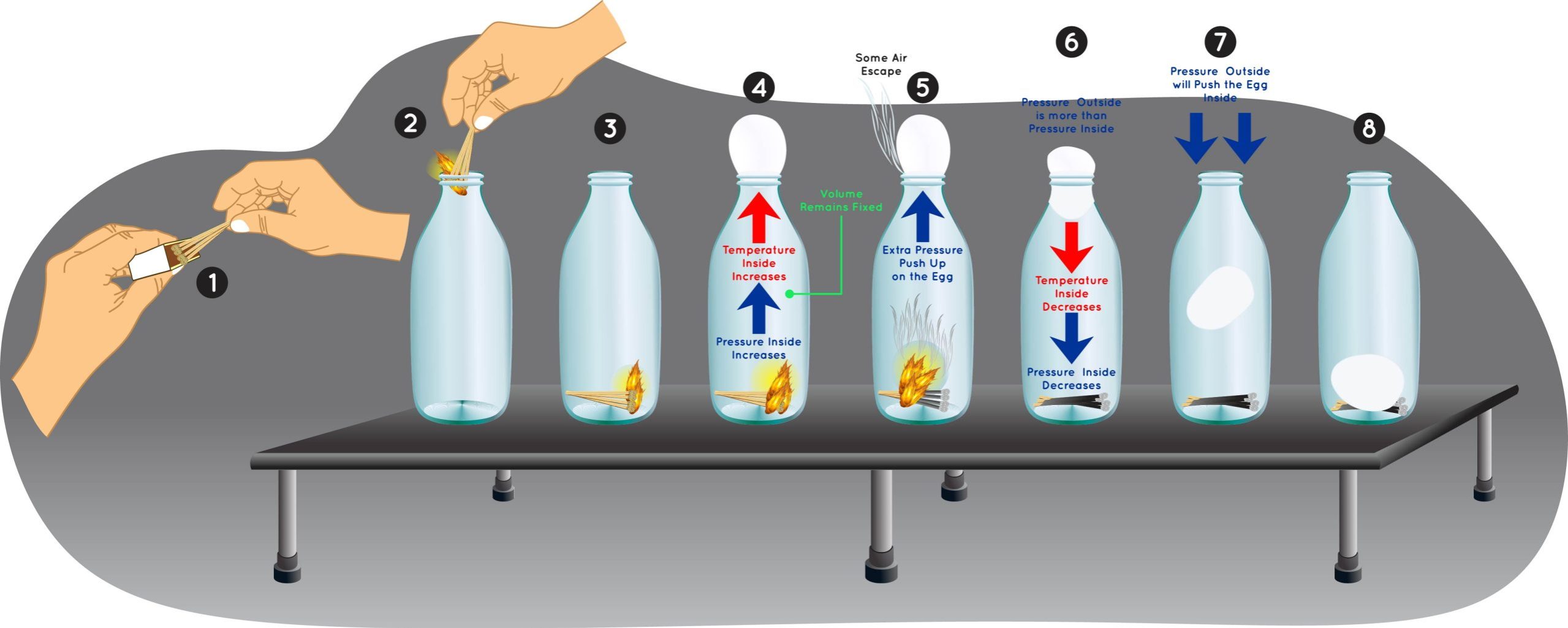
III. QUÁ TRÌNH ĐẲNG ÁP – ĐỊNH LUẬT CHARLES
1. Định luật Charles
Ở áp suất không đổi, thể tích của một khối lượng khí xác định tỉ lệ thuận với nhiệt độ tuyệt đối của nó.
\(\frac{V}{T} = \) hằng số
hay:
\(\frac{{{V_1}}}{{{T_1}}} = \frac{{{V_2}}}{{{T_2}}}\)
2. Đường đẳng áp
– Đường biểu diễn sự biến thiên của thể tích theo nhiệt độ khi áp suất không đổi gọi là đường đẳng áp.
– Trong hệ toạ độ (OV,OT), đường đẳng áp là đường thẳng kéo dài đi qua gốc toạ độ.
– Ứng với các thể tích khác nhau của cùng một lượng khí ta có những đường đẳng áp khác nhau.